今まで学んできた気体は、
などいろいろな気体が出てきて、とてもややこしいです。なのでこの回で簡単にまとめていきます。
ついでにもう一つ、よく出てくる気体の塩化水素もサラリと学べるようにしておきます。
気体の性質まとめ
まず、重要な5種類の気体を中心に見ていきます。
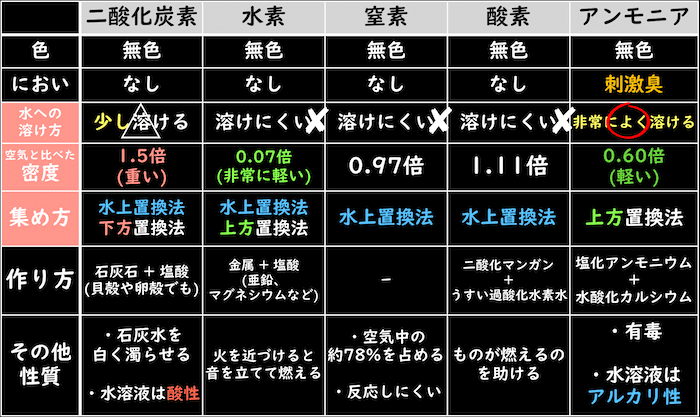
気体の色とにおい

二酸化炭素、窒素、酸素は大気中にたくさん含まれている物質です。
普段の生活では、空気の色やにおいは全く感じませんよね。なので、これら3つの気体には色もにおいもありません。
水素は、キャヴェンディッシュが発見した「燃える空気」です。飛行船を一瞬で焼き尽くしてしまう気体ですが、色とにおいがないことが逆に危険のもととなってますよね。
アンモニアは、ハーバーとボッシュが化学肥料のために空気から作ろうとした物質で、動物のおしっこにも含まれています。
ツンとする刺激臭があり、有毒なので取扱に注意する必要がある気体です。
空気と比べた密度、水への溶けやすさ、集め方

このあたりはセットで理解すると簡単ですね。
水の溶けやすさ
水の溶けやすさについては、
- 水に溶けにくい……水素、窒素、酸素
- 水に少し溶ける……二酸化炭素
- 水に非常によく溶ける……アンモニア
となります。(教科書がアホなところは、「水に溶けにくい」「水に少し溶ける」なんて曖昧な言葉を使っているところですね。「溶けにくい」「少し溶ける」の2つの言葉を並べても、どっちの方が溶けやすいのか普通は全然分かりません。)
水素と窒素と酸素はかなり水に溶けにくいですが、二酸化炭素は、水に少し溶けます。(水素/酸素/窒素に比べると、二酸化炭素はまだ水に溶ける方)
炭酸水は、二酸化炭素が水に溶けたものです。

例えばペットボトルに二酸化炭素と水を入れてよく振ると、ペットボトルがへこみます。
ボトル内の二酸化炭素が水に溶け込み、ボトル内の圧力が急に小さくなるからです。

アンモニアはとても水に溶けやすいので、水に溶かしてアンモニア水で保存することが多いですね。

気体の集め方
これらの純粋な気体を集めるためには、他の空気と混ざりにくい水上置換法を使うのが基本です。

これらの特性を考えると、アンモニア以外は水上置換法で実施できます。二酸化炭素は少し溶けますが、大きな問題はありません。
気体の密度(重さ)
次に、気体の密度(重さ)は、
- 空気より重い気体……二酸化炭素
- 空気と同じくらい……酸素、窒素
- 空気より軽い気体……水素、アンモニア
です。
これらを考えると、空気より重い二酸化炭素は下方置換法で集めることもできます。
空気より軽い水素とアンモニアは、上方置換法でもOKです。
アンモニアは水上置換法では集められないので、上方置換法でやるしかないですね。


気体の作り方

- 二酸化炭素……石灰石 + 塩酸。ブラックが発見
- 水素……金属(亜鉛など) + 塩酸。キャヴェンディッシュが発見
- 酸素……二酸化マンガン + うすい過酸化水素水(オキシドール)。プリーストリが発見
- アンモニア……塩化アンモニウム + 水酸化カルシウム。ハーバー・ボッシュ法が有名
その他の性質

この中では、火や物が燃えるのを助けるのは酸素だけです。二酸化炭素や窒素の中だと、火は燃えられずに消えてしまうことを、ブラックやシェーレが発見してましたよね。
水溶液が酸性になるのは二酸化炭素だけ。水に二酸化炭素が溶けた炭酸水は、酸性です。世界で始めて炭酸水を自作したのはプリーストリだったと言われています。

窒素は、空気の80%を占める気体で、あまり他と反応しないおとなしい性質です。何かを邪魔したりしないので、ポテトチップスなど食品の品質を保つために袋の中に注入されます。

塩素
塩素も大事な気体の一つですね。黄緑色をしていて、空気よりも2.5倍も重い気体です。

毒ガス、化学兵器として第一次世界大戦に利用されました。
しかしその毒性の強さを利用すれば、漂泊・殺菌作用のある物質として便利に利用できます。
よく塩素系漂白剤/洗浄剤が利用されていますが、その商品は決してお酢やアルコールなど酸性のものを混ぜないようにしましょう。塩素が発生してしまうからです!

他の液体とは隔離して使うのがいいでしょう。
塩化水素
最後に、塩化水素という気体も学んでおきます。

その名の通り、水素と塩素が化合した気体です。
ブラックやキャヴェンディッシュなどの化学者は、よく塩酸を利用していましたよね。

塩酸は金属でさえ溶かす、刺激臭のある危険な液体です。
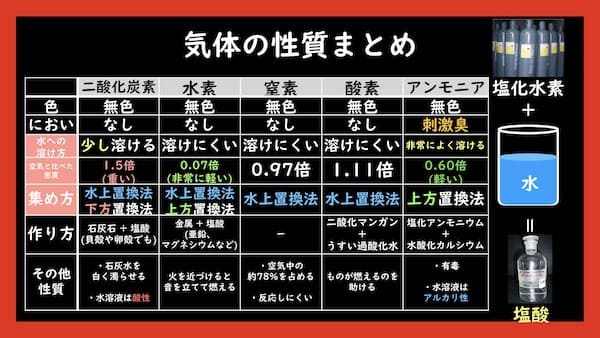
実は塩酸とは、塩化水素が水に溶けた液体のことなのです。塩化水素は、とても水に溶けやすいです。

塩化水素は無色ですが、強い刺激臭がします。塩酸の刺激臭は、塩化水素の性質のおかげです。
塩化水素の水溶液が塩酸ですが、塩酸は強い酸性を表すことを知っておいてください。






コメント